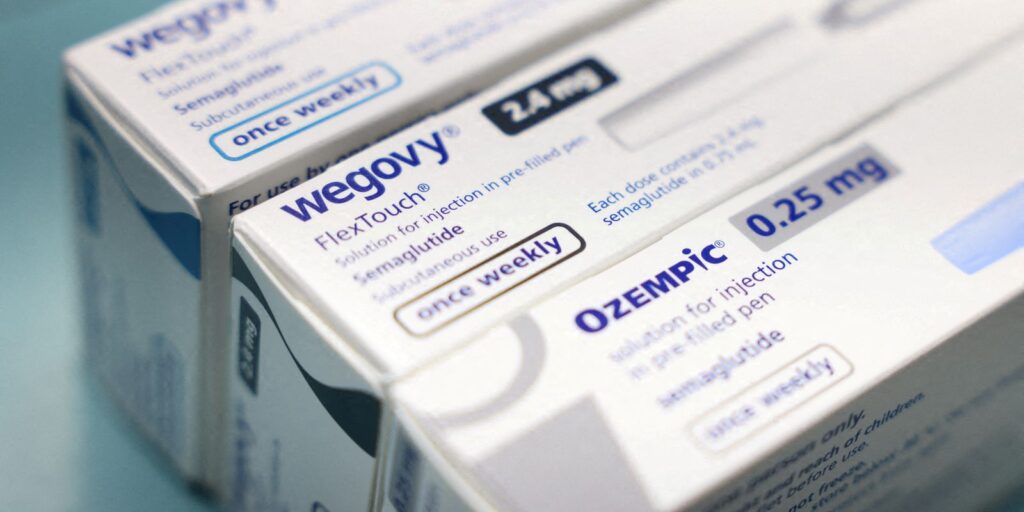
A patente da semaglutida, substância ativa utilizada em medicamentos como o Ozempic, chega ao fim nesta sexta-feira, dia 20. Essa mudança legal abre caminho para a produção de versões genéricas e biossimilares do medicamento, que é amplamente utilizado para o tratamento de diabetes tipo 2 e controle de peso. Com a expiração da patente, espera-se que novos produtos com preços mais acessíveis cheguem ao mercado, beneficiando uma parcela maior da população que depende de tratamentos eficazes.
Impacto da expiração da patente
A perda da proteção patentária da semaglutida é um marco importante no setor farmacêutico brasileiro. Atualmente, a Agência Nacional de Vigilância Sanitária (Anvisa) está avaliando oito processos para novos medicamentos que utilizam a mesma substância ativa. Esta situação pode não apenas aumentar a concorrência no mercado, mas também reduzir significativamente os preços para os consumidores.
Processos em análise
Segundo informações da Anvisa, dois desses processos estão em fase de exigência, o que significa que as empresas responsáveis precisam fornecer dados adicionais para que a análise prossiga. Os prazos para que as empresas respondam vão até o final de junho, o que impede a definição de um cronograma claro para a aprovação dos novos produtos.
Classificação dos medicamentos
Os medicamentos à base de semaglutida atualmente registrados no Brasil são classificados como produtos biológicos, e a nova legislação permite a entrada de medicamentos biossimilares e análogos sintéticos. Essa classificação é importante, pois define como os novos produtos serão avaliados e quais critérios de segurança e eficácia deverão ser atendidos.
Diferenças entre biossimilares e análogos sintéticos
Os biossimilares são obtidos por processos biológicos, enquanto os análogos sintéticos são produzidos através de síntese química. É crucial entender que, enquanto os biossimilares devem passar por rigorosas comparações com o produto original, os análogos sintéticos não têm a mesma categorização e podem ser avaliados sob diferentes critérios técnicos.
Desafios regulatórios
A Anvisa reconhece que a avaliação de análogos sintéticos da semaglutida representa um desafio técnico considerável. A não aprovação de produtos semelhantes nas principais agências de medicamentos do mundo, incluindo as dos Estados Unidos e da Europa, ressalta a complexidade do processo de avaliação. Para garantir a segurança dos pacientes, a análise deve considerar tanto os riscos associados a medicamentos sintéticos quanto as particularidades dos biológicos.
Critérios de avaliação
Os principais critérios de avaliação incluem a análise de impurezas, a formação de agregados, a garantia de esterilidade e a imunogenicidade. É fundamental que os novos medicamentos não causem reações adversas, como a formação de anticorpos que possam comprometer sua eficácia. A Anvisa está atenta a esses aspectos para assegurar a segurança dos novos produtos que possam ser lançados no mercado.
Decisão judicial sobre patentes
Em janeiro deste ano, o Superior Tribunal de Justiça decidiu não prorrogar o prazo de vigência das patentes do Ozempic e do Rybelsus, ambos contendo semaglutida. A ação foi movida pela empresa dinamarquesa Novo Nordisk, que buscava o reconhecimento de atrasos administrativos no processo de patente. A decisão do tribunal reafirma que o prazo de proteção patentária é de 20 anos a partir do depósito do pedido, sem possibilidade de prorrogação judicial.
A expiração da patente da semaglutida representa um avanço significativo na oferta de tratamentos acessíveis. Com a entrada de novos produtos no mercado, espera-se que mais pacientes possam ter acesso a medicamentos eficazes para o controle do diabetes e da obesidade, promovendo assim uma saúde pública mais inclusiva e justa.